2025-Week8 top papers in pathogenomics
病原微生物组学与智能算法前沿进展周报
1 微生物免疫机制
1.1 揭示噬菌体蛋白抑制宿主免疫的新机制
Structure-guided discovery of viral proteins that inhibit host immunity
Erez Yirmiya等,2025-1-23,Cell,链接
该研究开发了一种基于结构引导的计算流程,利用AlphaFold2结构预测工具,从超过3000万个噬菌体蛋白中系统性地筛选出能够抑制宿主免疫蛋白的病毒编码蛋白。研究重点关注了Thoeris和CBASS这两种细菌防御系统,它们分别是真核生物中Toll/interleukin-1 receptor (TIR) 和cyclic GMP-AMP synthase (cGAS) 免疫系统的祖先。研究发现了七个家族的Thoeris和CBASS抑制剂,这些抑制剂广泛存在于噬菌体中,并能够通过物理结合阻断免疫蛋白的活性位点。值得注意的是,噬菌体编码的细菌TIR蛋白抑制剂也能结合并抑制人类和植物的TIR,而噬菌体来源的细菌cGAS类酶抑制剂也能抑制人类cGAS。研究结果表明,噬菌体是免疫调节蛋白的宝库,能够抑制细菌、动物和植物的免疫系统。
- 开发系统性筛选流程 :利用AlphaFold2结构预测工具,开发了一种计算流程,能够从大规模的噬菌体蛋白数据库中识别出免疫调节蛋白。这一流程结合了降维过程和可靠性评估,能够有效筛选出细菌免疫蛋白的强效抑制剂,并进一步发现这些抑制剂也能结合并抑制人类和植物的免疫蛋白。
- 发现广泛存在的抑制剂家族 :发现了七个家族的Thoeris和CBASS抑制剂,这些抑制剂包含数千个基因,广泛存在于噬菌体中。这些抑制剂通过物理结合阻断免疫蛋白的活性位点,展现出对免疫系统的抑制作用。
- 揭示噬菌体抑制剂的跨物种抑制能力 :噬菌体编码的细菌TIR蛋白抑制剂能够结合并抑制人类和植物的TIR,噬菌体来源的细菌cGAS类酶抑制剂也能抑制人类cGAS,表明噬菌体抑制剂具有跨物种的免疫抑制能力。

1.2 修饰核苷酸介导细菌免疫信号通路
Base-modified nucleotides mediate immune signaling in bacteria
Zhifeng Zeng等,2025年2月20日,Science,链接
该研究揭示了一种细菌抗噬菌体系统,该系统通过核苷碱基修饰介导免疫信号。具体来说,噬菌体的核苷酸激酶与细菌系统编码的腺苷脱氨酶共同作用,产生脱氧肌苷三磷酸(dITP)作为免疫信使。dITP信号激活下游效应因子,导致细胞内NAD+耗竭,通过感染细胞的死亡实现群体水平的防御。为了对抗这种免疫信号,噬菌体则会部署专门的酶来消耗细胞内的dAMP,而dAMP正是dITP信使的前体。该研究发现了以核苷碱基修饰为基础的抗噬菌体信号通路,确立了非典型核苷酸作为细菌免疫信使的新类型。
1.3 巨噬细胞代谢再编程新机制
Macrophages recycle phagocytosed bacteria to fuel immunometabolic responses
Juliette Lesbats等,2025-02-26,Nature,链接
尽管吞噬作用在细菌感染中至关重要,但被吞噬的微生物的命运及其对宿主细胞的影响尚不清楚。研究通过追踪稳定同位素标记的细菌,发现被吞噬的细菌构成了一种替代营养源,影响了宿主的免疫代谢反应。具体来说,细菌在吞噬溶酶体中降解后,提供的碳原子和氨基酸被循环利用到多种代谢途径中,包括谷胱甘肽和顺乌头酸的生物合成,满足了巨噬细胞的生物能量需求。这种微生物衍生营养的代谢回收受到营养感应的雷帕霉素复合体C1(mTORC1)的调控,并且与微生物的活性密切相关。死细菌相较于活细菌,富含环腺苷酸,维持细胞内腺苷酸池,并激活腺苷酸蛋白激酶以抑制mTORC1。因此,被杀死的细菌强烈促进代谢回收,支持巨噬细胞存活,但与活细菌相比,产生的活性氧和白介素-1β分泌减少。这些结果为被吞噬微生物的命运提供了新见解,并强调了一种与微生物活性相关的代谢物,能够触发宿主的代谢和免疫反应,为免疫相关病理学的免疫代谢干预提供了新思路。
2 组学技术与病原监测
2.1 护理院皮肤耐药菌宏基因组分析
Clonal Candida auris and ESKAPE pathogens on the skin of residents of nursing homes
Diana M. Proctor等,2025-02-26,Nature,链接
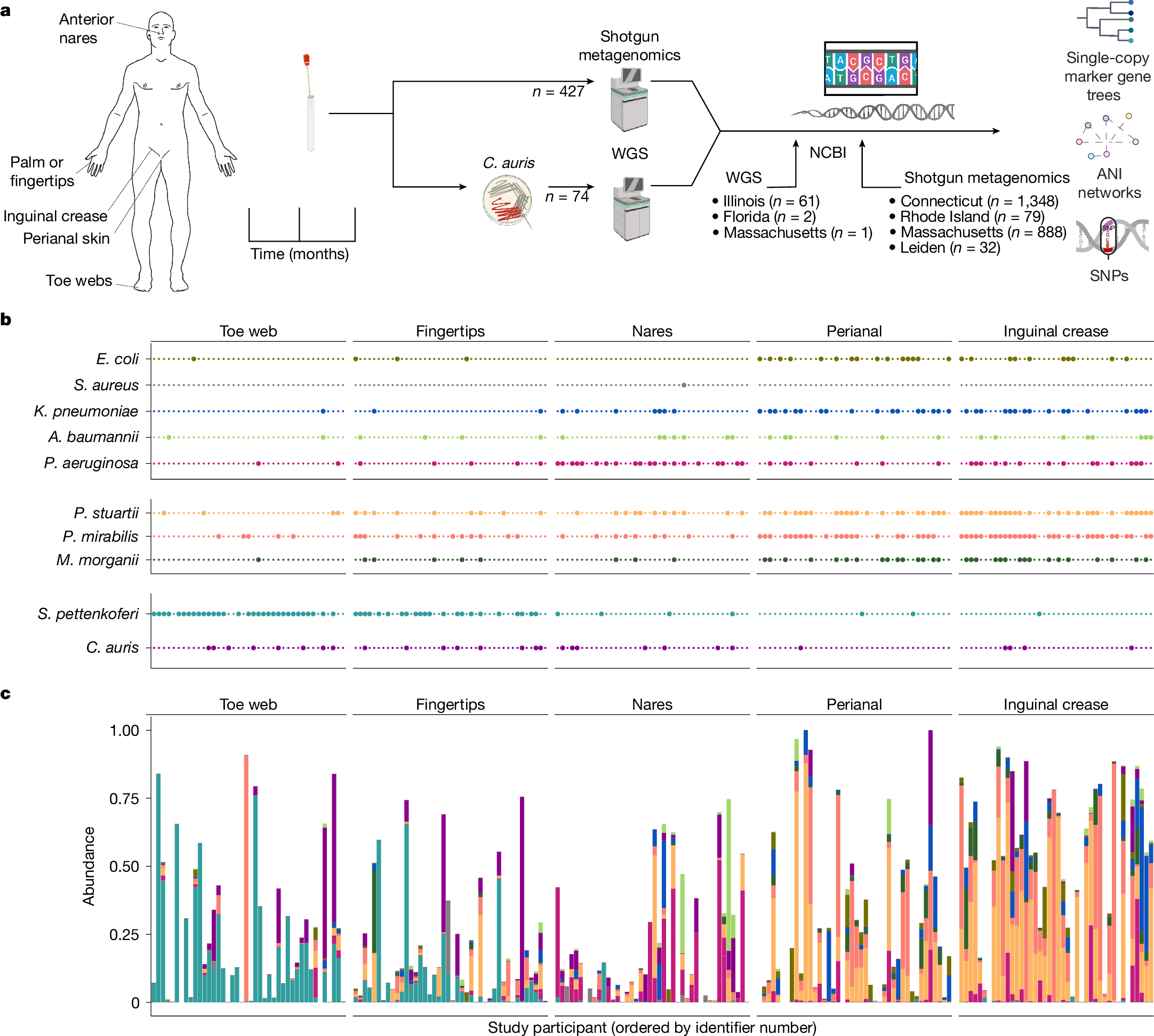
该研究聚焦于养老院中抗微生物耐药性问题,特别是新兴的多药耐药真菌病原体耳念珠菌(Candida auris)。研究结合菌株分辨宏基因组学和分离物测序,发现养老院居民皮肤上存在耳念珠菌的定植和克隆传播,并且这种传播在整个大都市区域都有发生。此外,研究还发现养老院中存在大量共享的耐药菌(包括 ESKAPE 路径病原体和其他高优先级病原体,如大肠杆菌、斯图尔特普罗维登西亚菌、奇异变形杆菌和摩根摩根菌)。通过整合微生物组和临床微生物学数据,研究在携带这些基因的居民多个皮肤部位检测到了碳青霉烯酶基因。对其他七个养老院居民的公开宏基因组样本(粪便和皮肤)进行分析,进一步提供了之前未被重视的细菌菌株共享的证据。总体而言,数据表明皮肤是耳念珠菌和 ESKAPE 病原体及其相关抗微生物耐药基因定植的储存库。
更多解读:解读Nature:养老院居民皮肤上的克隆耳念珠菌和ESKAPE病原体
2.2 肠道菌群恢复策略
Fuyong Li等,2025-01-23,Cell,链接
本文通过一项随机对照喂养试验,研究了一种模拟非工业化饮食模式的饮食干预策略对健康成年人肠道微生物组和宿主代谢的影响。
创新点
- 饮食干预策略 :提出了一种恢复肠道微生物组的饮食干预策略,包括模拟非工业化饮食模式的恢复饮食(restore diet)和一种在工业化微生物组中罕见的细菌(Limosilactobacillus reuteri)。
- 微生物组与宿主代谢的关联 :通过综合分析肠道微生物组和宿主代谢指标,揭示了饮食干预对肠道微生物组和宿主代谢的综合影响,以及微生物组特征与宿主代谢指标之间的关联。
新发现
- 恢复饮食对微生物组的影响 :恢复饮食降低了肠道微生物组的多样性,但增强了来自巴布亚新几内亚农村地区的 L. reuteri 菌株(PB-W1)的持久性,并纠正了工业化导致的多个微生物组特征的改变。
- 对宿主代谢的有益影响 :恢复饮食有益地改变了与慢性非传染性疾病发病机制相关的微生物群衍生血浆代谢物,独立于 L. reuteri 的给药,观察到了显著的心血管代谢益处,其中一些益处可以通过基线和饮食响应的微生物组特征准确预测。
- 微生物组特征的预测价值 :研究发现,肠道微生物组特征可以预测饮食的心血管代谢益处,这为通过微生物组特征预测宿主代谢变化提供了新的证据。

3 智能算法与合成生物学
3.1 可编程RNA靶向CRISPR系统进化
Reprogrammable RNA-targeting CRISPR systems evolved from RNA toxin-antitoxins
Shai Zilberzwige-Tal等,2025-02-18,Cell,链接
通过结构-序列联合挖掘揭示Cas13系统从RNA毒素-抗毒素系统进化而来,拓展CRISPR工具开发思路。
创新点
- 混合结构 - 序列搜索方法 :本研究采用了一种整合的序列 / 结构进化追踪方法,成功识别了 RNA 靶向 CRISPR-Cas13 系统的祖先,为研究 CRISPR 系统的进化起源提供了新的技术手段。
- 发现 Cas13 的祖先 :研究发现 Cas13 很可能从 AbiF 进化而来,AbiF 是由与中止感染相关的基因编码的,这一发现为理解 CRISPR 系统的进化历程提供了关键线索。
- 揭示 Cas13e 的中间地位 :鉴定出一种微型 Cas13(Cas13e),它在 AbiF 和其他已知 Cas13 之间起到了进化中间体的作用,有助于深入理解 Cas13 系统的进化过程。
- 结构解析 :通过冷冻电镜(cryo - EM)解析了 AbiF 的结构,揭示了 Cas13 与 AbiF 之间的基本结构差异,为研究 CRISPR 系统的结构与功能关系提供了重要基础。
新发现
- AbiF 的特性 :AbiF 是一个毒素 - 抗毒素(TA)系统,具有非编码 RNA(ncRNA)抗毒素,能够抑制 RNase 毒素,这一发现丰富了对 TA 系统的认识。
- Cas13e 的独特功能 :尽管 Cas13e 与 AbiF 存在进化关系,但它们的功能有显著差异。Cas13e 是一个 RNA 引导的 RNA 靶向系统,而 AbiF 是一个具有 RNA 抗毒素的 TA 系统,这表明在进化过程中,Cas13 系统的功能发生了重要转变。
- CRISPR 系统的进化机制 :研究揭示了从非引导的 TA 系统进化为 RNA 引导的 CRISPR 系统的关键结构变化,即 CRISPR RNA 结合和 REC 域的插入,这一发现对于理解 CRISPR 系统的进化机制具有重要意义。
3.2 丝氨酸水解酶计算设计
Computational design of serine hydrolases
Anna Lauko等,2025-02-13,Science,链接
整合RFdiffusion生成模型与集成采样方法,实现含复杂活性位点丝氨酸水解酶的从头设计。
3.3 多酶空间优化智能框架
Rational multienzyme architecture design with iMARS
Jiawei Wang等,2025-01-23,Cell,链接
开发iMARS标准化框架,将多酶体系空间优化从试错模式推进到理性设计阶段。

3.4 AI解析大肠杆菌蛋白质-代谢物互作网络**
Ligand interaction landscape of transcription factors and essential enzymes in E. coli
Hui Peng等,2025年1月24日,Cell,链接
蛋白 - 代谢物相互作用对于理解生物化学过程的机制和进行化学探针研究具有重要意义。然而,发现内源性配体(ligand)仍然具有挑战性。本研究结合了快速亲和纯化、精确质谱分析和高分辨率分子对接技术,精确绘制了 296 种化学多样性小分子代谢物配体与大肠杆菌中 69 种不同酶和 45 种转录因子的物理相互作用。
- 配体界面的功能意义:通过深入的 AI - 生物物理分析,揭示了配体界面的功能意义,包括网络水平上的功能串扰原理、结合口袋的保守性模式以及设计选择性化学探针的支架。
- 进化关系:研究还发现了不同酶和转录因子在进化过程中的结合口袋保守性模式,为理解这些蛋白在不同物种中的进化关系提供了重要信息。
本研究开发的结构解析配体互作组图谱绘制流程,可以扩展到完整细胞甚至整个多细胞群落的本土小分子网络研究,为未来的研究提供了新的方法和思路。研究结果为设计选择性合成化学探针提供了支架,有助于开发新的化学工具来研究生物化学过程。
创新点
- 高置信度鉴定:开发了一种高置信度鉴定本土蛋白 - 配体相互作用的流程,提高了鉴定的准确性和可靠性。
- 多技术整合:将快速亲和纯化、精确质谱分析和高分辨率分子对接等多种技术整合,实现了对蛋白 - 配体相互作用的精确绘制。
- 深入的生物物理分析:通过 AI - 生物物理分析,深入揭示了配体界面的功能意义,为理解蛋白 - 代谢物相互作用提供了新的视角。
4 冠状病毒研究进展
4.1 蝙蝠源HKU5冠状病毒ACE2趋同进化
Young-Jun Park等,2025-02-07,Cell,链接
发现多个merbecovirus谱系独立进化出ACE2利用能力,揭示冠状病毒受体转换的分子基础。
4.2 新型冠状病毒融合中间态靶点
Lixiao Xing等,2025-01-30,Cell,链接
解析ACE2诱导的刺突蛋白早期融合中间态结构,开发出广谱抗冠状病毒工程蛋白AL5E。
总结
本周研究聚焦微生物免疫机制解析(细菌核苷酸信号、巨噬细胞代谢重塑)、组学技术临床转化(耐药菌传播追踪、菌群重建策略)、智能算法突破(CRISPR进化解析、酶理性设计、多酶优化框架)三大方向。冠状病毒研究持续深入,揭示受体转换的趋同进化规律,为广谱抗病毒药物开发提供新靶点。人工智能与合成生物学深度融合,推动生物制造与基因编辑技术革新。